 2009-11-14, 11:17
2009-11-14, 11:17
|
رقم المشاركة : 13
|
 معلومات
العضو معلومات
العضو |
|
|
 إحصائية
العضو إحصائية
العضو |
|
|
|
 اعادة شرح
اعادة شرح
لم اجد الشرح في المرة السابقة لذا وجدت شرحا في هذه المرة.
Du fait de la présence de liaisons riches en énergieروابط غنية بالطاقة (celles liant les groupements phosphate sont des liaisonsanhydride phosphorique), cette molécule est utilisée chez les êtres vivants pour fournir de l'énergie aux réactions chimiques qui en consomment. L'ATP est la réserve d'énergie de la cellule(اي هو اين تخزن طاقة الخلية ) .
En effet, la réaction d'hydrolyse de l'adénosine triphosphate en adénosine diphosphate et phosphate est une réaction exergonique : la variation d'enthalpie libre standard est égale à −30,5 kJ/mol
وهنا في هذا المثال كما راينا في الرابطة بين الحمض الاميني وARNT حيث تستعمل ATP فتستعمل منها PI فقط وتبقى ADP :
 Au contraire, la réaction de synthèse de l'adénosine triphosphate à partir d'adénosine diphosphate et de phosphate est une réaction endergonique : la variation d'enthalpie libre standard est égale à +30,5 kJ/mol :
Au contraire, la réaction de synthèse de l'adénosine triphosphate à partir d'adénosine diphosphate et de phosphate est une réaction endergonique : la variation d'enthalpie libre standard est égale à +30,5 kJ/mol :
 La réaction d'hydrolyse de l'ATP en adénosine monophosphate (et pyrophosphate) est une réaction exergonique : la variation d'enthalpie libre standard est égale à −42 kJ/mol :
La réaction d'hydrolyse de l'ATP en adénosine monophosphate (et pyrophosphate) est une réaction exergonique : la variation d'enthalpie libre standard est égale à −42 kJ/mol :
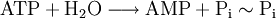 L'énergie est donc stockée dans les liaisons entre les groupements phosphate.
Il existe cependant un palier d'enthalpie à franchir avant de libérer cette énergie (état de transition). Ceci explique que l'hydrolyse des liaisons pyrophosphate ne se produise pas en permanence. Les enzymes sont capables d'abaisser ce seuil, afin d'utiliser l'énergie libérée.
Si l'énergie est ainsi stockée dans les liaisons anhydrides, on peut se demander quel est l'intérêt pour les êtres vivants de synthétiser la molécule entière, et non uniquement des pyrophosphate libres. La réponse est probablement dans la capacité des enzymes à reconnaitre l'ATP, plus aisé à hydrolyser spécifiquementbiomolécules. que des pyrophosphate libres, très semblables à tous les groupements phosphate présents dans les
L'énergie est donc stockée dans les liaisons entre les groupements phosphate.
Il existe cependant un palier d'enthalpie à franchir avant de libérer cette énergie (état de transition). Ceci explique que l'hydrolyse des liaisons pyrophosphate ne se produise pas en permanence. Les enzymes sont capables d'abaisser ce seuil, afin d'utiliser l'énergie libérée.
Si l'énergie est ainsi stockée dans les liaisons anhydrides, on peut se demander quel est l'intérêt pour les êtres vivants de synthétiser la molécule entière, et non uniquement des pyrophosphate libres. La réponse est probablement dans la capacité des enzymes à reconnaitre l'ATP, plus aisé à hydrolyser spécifiquementbiomolécules. que des pyrophosphate libres, très semblables à tous les groupements phosphate présents dans les
|
|
|

|